Một sản phẩm muốn được cấp phép là thuốc cần phải qua một quá trình nghiên cứu phát triển rất phức tạp, qua nhiều chặng. Mỗi chặng lại có những yêu cầu đánh giá chặt chẽ để xem sản phẩm đó có đạt yêu cầu rồi mới được chuyển tiếp sang những chặng tiếp theo. Quy chuẩn đánh giá cho các chặng trong quá trình nghiên cứu phát triển này mang tính toàn cầu hóa.
Các bước nghiên cứu thuốc cần có
Nghiên cứu phát triển thuốc có thể tóm tắt qua 3 chặng chính:
Khám phá:
Các nhà nghiên cứu tìm kiếm các chất có thể có tác dụng điều trị cho người.
Nghiên cứu tiền lâm sàng:
Các chất là ứng viên tiềm năng sàng lọc ở chặng 1 sẽ được thử nghiệm trên các tế bào/các mô hình trong phòng thí nghiệm và/hoặc trên động vật thí nghiệm. Chặng này gồm nhiều nghiên cứu khác nhau nhằm xác định tính an toàn của sản phẩm nghiên cứu ví dụ như độc tính cấp, độc tính trên các cơ quan, khả năng gây ung thư/đột biến/quái thai…
Đồng thời cũng từ chặng này, các đặc tính cơ bản của một "thuốc" trong tương lai bắt đầu được hình thành, như cơ chế tác dụng, liên quan giữa liều và đáp ứng, động học, tương tác…
Nếu sản phẩm nghiên cứu đáp ứng được những quy chuẩn cho thấy, có thể sẽ là một phương pháp điều trị hiệu quả và đặc biệt là đáp ứng những quy chuẩn về an toàn, sản phẩm đó sẽ cần xin cấp phép để chuyển sang chặng 3 – chặng nghiên cứu trên con người, hay còn gọi là chặng Thử nghiệm lâm sàng.

Một sản phẩm muốn được cấp phép là thuốc phải qua một quá trình nghiên cứu phát triển rất phức tạp.
Thử nghiệm lâm sàng:
Chặng này gồm 3 giai đoạn (hay còn gọi là 3 pha). Mỗi giai đoạn lại gồm nhiều nghiên cứu đặc thù khác nhau với mục tiêu, cỡ mẫu và thiết kế nghiên cứu chặt chẽ theo quy định. Các giai đoạn này được thiết kế nối tiếp, bài bản, chặt chẽ để trả lời các câu hỏi về tính an toàn khi dùng trên người, tìm kiếm mức liều dùng phù hợp, xác định các đặc tính và đặc biệt là thử nghiệm xem sản phẩm nghiên cứu có thực sự chứng minh được hiệu quả như mong đợi hay không.
Sau khi đi hết giai đoạn 3, nếu các kết quả thử nghiệm đạt yêu cầu, sản phẩm nghiên cứu mới hoàn thiện hồ sơ xin cấp phép là "Thuốc".
Tổng kết lại lịch sử nghiên cứu phát triển thuốc toàn cầu, trong chặng Khám phá, thường phải sàng lọc từ 5.000 đến 10.000 chất để có thể có được khoảng 250 chất đưa vào chặng nghiên cứu tiền lâm sàng.
Trong 250 chất đó trung bình không có tới 10 loại có đủ tiềm năng để cấp phép đưa vào thử lâm sàng giai đoạn 1 trên người.
Và trong khoảng 10 loại chất thử lâm sàng trên người, trung bình chỉ 1 chất đi được qua đủ 3 giai đoạn thử nghiệm lâm sàng để xin cấp phép là thuốc.
Vì thế, nếu tính cho cả một quá trình nghiên cứu phát triển, trung bình thường mất khoảng 10-15 năm kể từ giai đoạn Khám phá ban đầu cho tới khi có 1 thuốc đưa vào điều trị cho người bệnh. Chi phí trung bình cho việc nghiên cứu và phát triển thành công một thuốc vào khoảng 800 triệu đôla cho tới 1 tỷ đô la.
Những nhầm lẫn cần làm rõ
Một sản phẩm đã hoàn thành giai đoạn nghiên cứu tiền lâm sàng là một ứng viên tiềm năng trở thành thuốc điều trị. Tuy nhiên vẫn có một xác suất rất cao chất đó không chứng minh được hiệu quả an toàn qua các thử nghiệm lâm sàng, và không thể trở thành thuốc. Do vậy không bao giờ được nhầm lẫn giữa một sản phẩm thử nghiệm lâm sàng với thuốc.
Sản phẩm đưa vào thử nghiệm lâm sàng cũng chưa thể khẳng định được sẽ có hiệu quả gì, dùng với liều bao nhiêu, trong thời gian như thế nào, cần theo dõi những gì, tác dụng phụ ra sao…
Vì vậy, một sản phẩm đưa vào thử nghiệm lâm sàng nói chung chỉ nên đặt tên bằng mã số nghiên cứu, không nên thiết kế nhãn với các thông tin như một thuốc đã được cấp phép lưu hành. Và đương nhiên các thông tin ban đầu nếu đưa vào nhãn của sản phẩm thử nghiệm này sẽ không chính xác bởi mục đích của thử nghiệm lâm sàng chính là nhằm tìm ra các thông tin, các đặc tính của thuốc để đưa lên nhãn.

Một sản phẩm đưa vào thử nghiệm lâm sàng nói chung chỉ nên đặt tên bằng mã số nghiên cứu, không nên thiết kế nhãn với các thông tin như một thuốc đã được cấp phép lưu hành.
Sản phẩm thử lâm sàng là sản phẩm chỉ được sản xuất cho duy nhất mục đích thử nghiệm, cấm dùng vào mục đích khác. Vì vậy sẽ không bao giờ các sản phẩm thử nghiệm này được phép sản xuất, kinh doanh dưới bất kỳ hình thức nào. Vì vậy, người dân không nên mới nghe tin có chế phẩm nghiên cứu thành công giai đoạn tiền lâm sàng đã vội vàng đổ xô đi tìm mua, tích trữ, và cẩn thận sẽ gặp phải các sản phẩm giả mạo là thuốc.
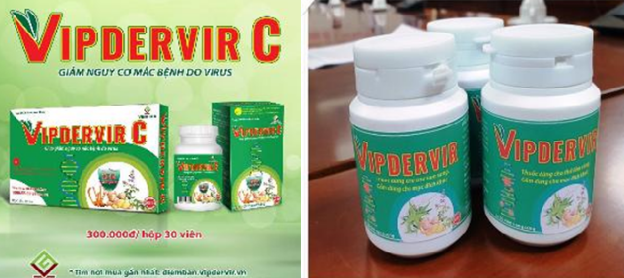
Nhãn của sản phẩm thử nghiệm lâm sàng không nên thiết kế tương tự nhãn của một thực phẩm chức năng, có thể gây nhầm lẫn cho người tiêu dùng
Xem thêm video đang được quan tâm:
Bộ Y tế điểm danh các tỉnh tiêm vaccine ngừa COVID-19 chậm | #tiemvaccine #Ho_Chi_Minh #BỘ_Y_TẾ




