1. Ukoniq là thuốc gì?
Ukoniq (umbralisib) là thuốc đã được phê duyệt để điều trị hai loại ung thư hạch (còn gọi là u lympho hay ung thư hạch bạch huyết - loại ung thư ảnh hưởng đến hệ thống miễn dịch của cơ thể). Cụ thể:
- Ukoniq là thuốc kê đơn được phê duyệt để điều trị người lớn bị ung thư hạch vùng biên (MZL) khi bệnh đã tái phát hoặc không đáp ứng với điều trị trước đó bằng ít nhất một loại thuốc cụ thể.
- Ukoniq cũng được chấp thuận để điều trị cho người lớn bị ung thư hạch bạch huyết dạng nang (FL) khi bệnh đã trở lại hoặc không đáp ứng với ít nhất ba lần điều trị trước đó.
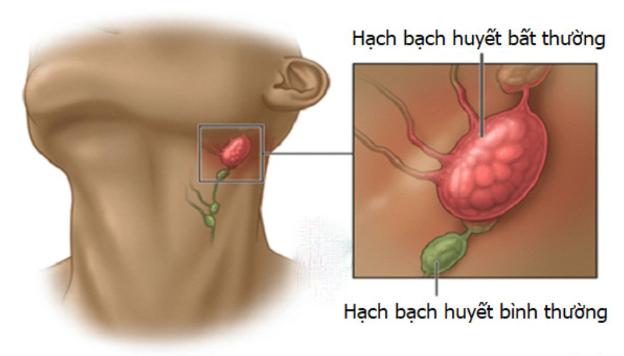
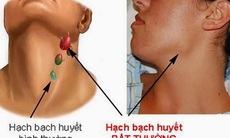
Hạch bạch huyết bình thương và bất thường.
FDA xác định rằng những phát hiện ban đầu từ một thử nghiệm lâm sàng đánh giá ukoniq để điều trị một loại ung thư liên quan cho thấy nguy cơ tử vong có thể tăng lên ở những bệnh nhân dùng thuốc.
Do mức độ nghiêm trọng của mối quan tâm an toàn này và sự tương đồng giữa hai loại ung thư mà loại thuốc này được phê duyệt và loại ung thư đã được nghiên cứu trong thử nghiệm lâm sàng, FDA cảnh báo cho bệnh nhân và các chuyên gia chăm sóc sức khỏe rằng FDA đang tái đánh giá rủi ro này so với lợi ích của ukoniq đối với các mục đích sử dụng đã được phê duyệt.
FDA đang tiếp tục đánh giá kết quả từ thử nghiệm lâm sàng mang tên UNITY và có thể tổ chức một cuộc họp công khai trong tương lai để thảo luận về những phát hiện này và tiếp tục theo dõi tính an toàn của thuốc ukoniq.
FDA cũng đã đình chỉ việc tiếp nhận bệnh nhân mới trong các thử nghiệm lâm sàng đang diễn ra khác của ukoniq trong khi cơ quan này tiếp tục xem xét các phát hiện của UNITY và sẽ thông báo kết luận và khuyến nghị cuối cùng của khi hoàn thành việc xem xét hoặc có thêm thông tin để chia sẻ.
FDA đã tiến hành đánh giá ban đầu dữ liệu từ UNITY, giai đoạn 3, thử nghiệm lâm sàng ngẫu nhiên, có đối chứng ở bệnh nhân mắc bệnh bạch cầu lymphocytic mãn tính (CLL). Thử nghiệm đang đánh giá ukoniq kết hợp với một loại thuốc kháng thể đơn dòng nhắm vào một protein cụ thể được gọi là CD20 so với nhánh đối chứng mà bệnh nhân được điều trị tiêu chuẩn.
Kết quả cho thấy nguy cơ tử vong có thể gia tăng ở những bệnh nhân dùng kết hợp ukoniq và kháng thể đơn dòng so với nhóm đối chứng. Những người nhận được sự kết hợp của ukoniq và kháng thể đơn dòng cũng gặp phải các tác dụng phụ nghiêm trọng hơn so với những người ở nhóm đối chứng.
Người bệnh cần theo dõi tác dụng phụ của thuốc có thể xảy ra trong quá trình sử dụng.
Thử nghiệm UNITY được thực hiện trên bệnh nhân CLL, không phải là cách sử dụng đã được phê duyệt mà là việc sử dụng cho nghiên cứu. Tuy nhiên, FDA tin rằng những phát hiện này có ý nghĩa đối với việc sử dụng nó đã được phê duyệt đối với bệnh ung thư hạch vùng biên (MZL) và ung thư hạch dạng nang (FL). Ngoài ra, các thử nghiệm lâm sàng về các loại thuốc khác trong cùng nhóm chất ức chế PI3 kinase như ukoniq đã cho thấy mối quan tâm về an toàn tương tự.
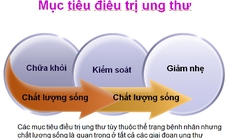
2. Một số khuyến nghị khi dùng thuốc trị ung thư hạch
- Các chuyên gia chăm sóc sức khỏe nên xem xét sự tiến triển của bệnh nhân đối với ukoniq và thảo luận với họ về những rủi ro và lợi ích của việc tiếp tục sử dụng ukoniq trong bối cảnh các phương pháp điều trị có sẵn khác.
- Đối với bệnh nhân nên trao đổi với bác sĩ về các rủi ro và lợi ích của ukoniq hoặc bất kỳ mối quan tâm nào bạn có thể có, bao gồm cả về các phương pháp điều trị thay thế có thể có.
- Các chuyên gia chăm sóc sức khỏe, người tiêu dùng và bệnh nhân được khuyến khích báo cáo các sự kiện bất lợi hoặc tác dụng phụ liên quan đến việc sử dụng các sản phẩm này cho các cơ quan liên quan.
Mời độc giả xem thêm video:
F0 vẫn tăng, WHO kêu gọi các nước không dỡ bỏ toàn bộ biện pháp chống dịch