Theo hãng tin BBC, ngày 4/11 trong một tuyên bố đại diện Bộ Y tế Anh thông báo, Anh trở thành nước đầu tiên trên thế giới cấp phép có điều kiện cho Molnupiravir - thuốc điều trị bệnh COVID-19 có triệu chứng do hai hãng dược Merck và Ridgeback Biotherapeutics cùng phát triển.
“Hôm nay là ngày lịch sử đối với đất nước chúng ta khi Anh là nước đầu tiên trên thế giới phê duyệt thuốc chống virus có thể được sử dụng tại nhà cho bệnh nhân COVID-19”, Bộ trưởng Y tế Anh Sajid Javid thông báo.
Thông báo trên được đưa ra sau khi Cơ quan Quản lý Dược phẩm và Sản phẩm Chăm sóc Sức khỏe Anh (MHRA) phê duyệt sử dụng thuốc viên kháng virus Molnupiravir để điều trị cho bệnh nhân COVID-19 nhẹ và trung bình. Dự kiến thuốc Molnupiravir sẽ tạo ra bước ngoặt trong điều trị COVID-19.
"Đây sẽ là yếu tố thay đổi cuộc chơi đối với những người dễ bị tổn thương nhất và bị ức chế miễn dịch. Họ sẽ sớm được nhận phương pháp điều trị mang tính đột phá", ông Javid cho biết thêm.

Thuốc Molnupiravir là một thuốc kháng virus sử dụng qua đường uống dùng để trị COVID-19. Ảnh: CNBC
Thuốc Molnupiravir là thuốc kháng virus đường uống chuyên dụng đầu tiên dành cho bệnh nhân COVID-19, được phát triển bởi Công ty dược phẩm Merck của Mỹ. Molnupiravir hoạt động bằng cách giảm khả năng sinh sôi của virus, có tác dụng giảm gần 50% nguy cơ bệnh nhân COVID-19 phải nhập viện và tử vong.
MHRA cho biết các thử nghiệm của họ cho thấy thuốc an toàn và có hiệu quả giảm nguy cơ nhập viện và tử vong ở ca COVID-19 từ nhẹ đến trung bình, những người có nguy cơ phát triển triệu chứng nặng.
Các dữ liệu thử nghiệm lâm sàng chỉ rõ, thuốc hiệu quả nhất khi được dùng trong giai đoạn đầu mắc COVID-19 và MHRA khuyến cáo sử dụng thuốc trong vòng 5 ngày kể từ khi bắt đầu xuất hiện triệu chứng. Thuốc cũng được cấp phép sử dụng cho người có ít nhất một yếu tố nguy cơ phát triển bệnh nặng, gồm béo phì, cao tuổi, tiểu đường và bệnh tim.
Tại thị trường Anh, loại thuốc trên sẽ được bán với nhãn hiệu là Lagevrio. Sau khi MHRA cấp phép, Chính phủ Anh và Cơ quan Dịch vụ y tế quốc gia Anh (NHS) sẽ công bố cách thức điều trị cho các bệnh nhân.
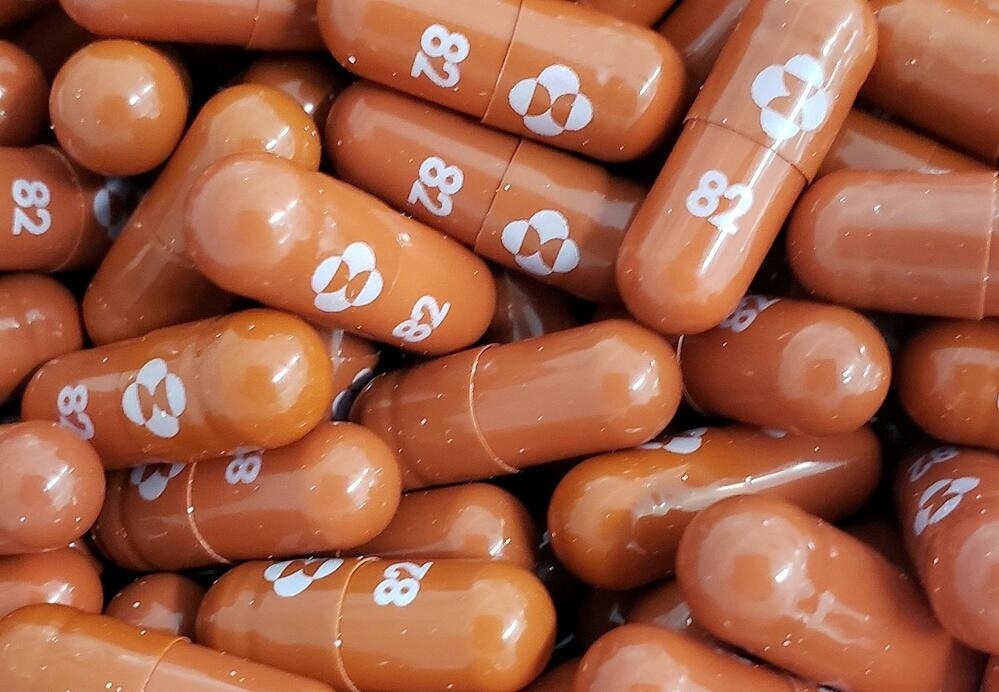
Thuốc kháng virus Molnupiravir do hai Công ty Merck và Ridgeback Biotherapeutics phát triển. Ảnh: Reuters
Tại Mỹ, hãng dược phẩm Merck và đối tác Ridgeback Biotherapy cũng đang yêu cầu Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) cấp phép sử dụng khẩn cấp loại thuốc này cho người lớn mắc COVID-19 từ mức độ nhẹ đến trung bình, cho những người có nguy cơ mắc bệnh nặng hoặc phải nhập viện.
Lãnh đạo cấp cao của Merck là Tiến sĩ Nicholas Kartsonis cho biết: "Giá trị nằm ở chỗ viên thuốc này giúp bạn không phải đến bệnh viện và đối mặt với những nguy cơ khác. Tôi nghĩ đây là một công cụ cực mạnh".
Đầu tháng 10 vừa qua, hãng dược phẩm Merck ghi nhận thuốc Molnupiravir đã giảm một nửa số ca nhập viện và tử vong ở những bệnh nhân có các triệu chứng ban đầu của COVID-19. Nếu được cấp phép, bệnh nhân COVID-19 có thể sử dụng loại thuốc uống này để điều trị tại nhà, nhằm giảm các triệu chứng và tăng tốc độ bình phục. Đồng thời có thể giúp giảm tải áp lực đối với các bệnh viện tại Mỹ và hạn chế bùng phát đại dịch ở các nước nghèo vốn có hệ thống y tế yếu kém.
Merck cho biết họ dự kiến sản xuất 10 triệu liệu trình điều trị vào cuối năm nay và thêm ít nhất 20 triệu liệu trình vào năm 2022.
Xem thêm video đang được quan tâm
Thích ứng an toàn, linh hoạt, kiểm soát hiệu quả dịch COVID-19