Nhưng sự xuất hiện của vi khuẩn đa kháng thuốc do lạm dụng kháng sinh đang làm dấy lên lo ngại rằng đến năm 2050, những bệnh do nhiễm khuẩn sẽ một lần nữa trở thành nguyên nhân gây tử vong hàng đầu trên toàn thế giới. Mới đây, các nhà khoa học đã lập trình thành công cấu trúc di truyền của vi khuẩn, có thể chống lại tình trạng kháng thuốc này.
Sự thất bại của kháng sinh
Việc phát hiện ra kháng sinh vào những năm 1930 đã mở đường cho sự tiến bộ về y tế và xã hội chưa từng có. Nhưng 20 năm qua đã chứng kiến sự xuất hiện của các cơ chế kháng vi khuẩn đang lan rộng khắp hành tinh. Rất ít loại kháng sinh mới được phát triển và thời gian từ khi đưa ra phương pháp điều trị cho đến khi có được tình trạng kháng thuốc sau đó trở nên ngắn hơn. Kháng thuốc gây nguy hiểm cho khả năng điều trị các bệnh truyền nhiễm dẫn đến tàn tật và tử vong. Hơn nữa, khi điều trị bằng kháng sinh, các phân tử trị liệu sẽ tấn công tất cả các vi khuẩn, kể cả vi khuẩn có lợi. Sự phá hủy không nhắm mục tiêu này sẽ dẫn đến rối loạn sinh lý, nói cách khác là phá vỡ sự cân bằng của hệ sinh thái vi khuẩn có thể dẫn đến sự xuất hiện của vi khuẩn kháng kháng sinh.
Tác động có hại đó có thể được ngăn chặn bằng cách phát triển các chiến lược kháng khuẩn đặc hiệu cao. Ví dụ, công cụ CRISPR-Cas9 có thể được sử dụng để nhắm mục tiêu vào các gene kháng thuốc ở vi khuẩn gây bệnh nhưng tỷ lệ thất bại liên quan đến kỹ thuật này (khi mầm bệnh tìm cách thoát khỏi các cơ chế phòng vệ khác nhau được sử dụng bởi sinh vật bị nhiễm bệnh) là tương đối cao.
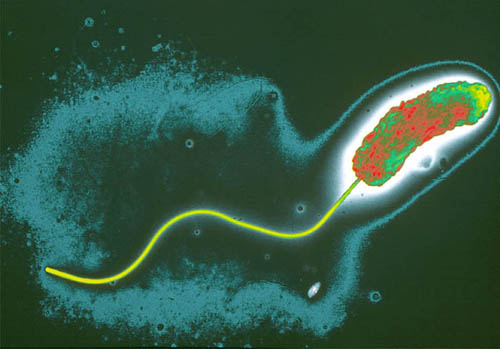
Hình ảnh vi khuẩn Vibrio cholerae.
Tín hiệu đáng mừng
Trong nỗ lực này, một nhóm các nhà khoa học dẫn đầu là GS. Didier Mazel - Viện Pasteur đã phát triển một chiến lược thay thế dựa trên biểu hiện cụ thể của các độc tố cực kỳ mạnh được phân phối bằng cách kết hợp. Sự kết hợp này là một quá trình được vi khuẩn sử dụng để trao đổi gene thông qua các Plasmid - các phân tử DNA đặc trưng cho bộ gene của vi khuẩn. Trong chiến lược mới này, gene mã hóa chất độc nằm trong Plasmid. “Việc sử dụng độc tố từ độc tố typ II (trong hệ thống độc tố) có vẻ như là một ý tưởng tốt vì dường như vi khuẩn không phát triển sức đề kháng đến kho vũ khí này. Nhưng một trong những thách thức của phương pháp này là làm thế nào để kiểm soát sức mạnh tuyệt đối của những chất độc này. Chúng tôi đã làm điều này bằng cách tách gene của chúng thành 2 mảnh để đảm bảo rằng chúng sẽ chỉ hiệu quả nếu hai phần có thể được kết hợp lại”, Didier Mazel - tác giả chính của bài báo giải thích.
Các nhà khoa học đã xác minh tính chất đặc biệt của chất độc này trong Vibrio cholerae - một loại vi khuẩn gram âm gây bệnh tả ở người. “Trước tiên, chúng tôi muốn kích hoạt biểu hiện độc tố trong Vibrio cholerae bằng cách sử dụng một chất khởi động được vi khuẩn này đặc biệt công nhận và kích hoạt phức hợp độc tố”, Didier Mazel cho biết. Sau đó, các nhà nghiên cứu đã tinh chế “vũ khí” này để độc tố chỉ có thể nhắm mục tiêu vào các chủng Vibrio cholerae kháng kháng sinh. Điều này liên quan đến việc tạo ra một mô-đun di truyền biểu hiện một chất ức chế độc tố đặc hiệu cao, đó là chất chống độc, không còn được sản xuất khi vi khuẩn chứa gene kháng thuốc. Bằng cách kết hợp 2 quy trình này, họ đã phát triển một cấu trúc di truyền có hiệu quả được xác minh trong các cộng đồng vi khuẩn tự nhiên phức tạp trong các vi khuẩn zebrafish và artemia.
Didier Mazel nói: “Mức độ thất bại của chiến lược thay thế này là rất thấp. Nó có thể dễ dàng thích nghi với sự tiêu diệt cụ thể của một số mầm bệnh. Tuy nhiên, để đạt được kết quả tốt nhất, chúng tôi còn phải tiến hành nhiều nghiên cứu nữa, đặc biệt là việc cải thiện quá trình chuyển gene của Plasmid”. Hy vọng với những tín hiệu đáng mừng này, trong tương lai không xa, cuộc chiến với vi khuẩn kháng thuốc sẽ trở nên dễ dàng hơn.