Mới đây, Cơ quan Quản lý thực phẩm và dược phẩm Mỹ (FDA) cho biết, cơ quan này đã tăng cường cảnh báo về những nguy cơ hiện có gây tổn thương thận cấp tính đối với các loại thuốc trị tiểu đường typ 2 canagliflozin (invokana, invokamet) và dapagliflozin (farxiga, xigduo XR). Dựa trên các báo cáo gần đây, FDA đã điều chỉnh lại những lời cảnh báo trên nhãn thuốc bao gồm thông tin về tổn thương thận cấp tính và kiến nghị bổ sung để giảm thiểu nguy cơ này.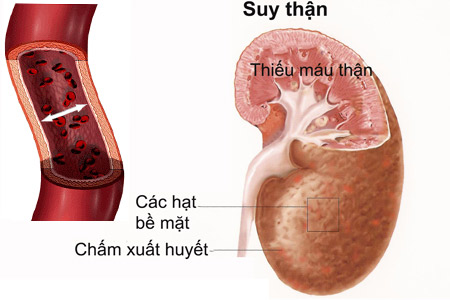
Suy thận do thuốc trị tiểu đường.
Bệnh nhân nên tìm kiếm sự chăm sóc y tế ngay lập tức nếu gặp phải các dấu hiệu và triệu chứng của tổn thương thận cấp tính. Vì đây là một tình trạng nghiêm trọng, làm thận đột ngột ngừng hoạt động khiến cho các chất thải bị tích tụ trong cơ thể sẽ gây nguy hiểm. Các dấu hiệu và triệu chứng của tổn thương thận cấp tính có thể bao gồm giảm nước tiểu hoặc sưng ở chân hoặc bàn chân. Tuy nhiên, FDA khuyên đối với bệnh nhân đang dùng thuốc, không nên ngừng uống thuốc nếu không có ý kiến của bác sĩ. Vì việc tự ý ngừng thuốc sẽ làm cho lượng đường trong máu không kiểm soát được, gây biến chứng.
Đối với bác sĩ, nên xem xét các yếu tố nguy cơ của bệnh nhân có thể dẫn tới hoặc làm nặng hơn tổn thương thận cấp tính trước khi bắt đầu sử dụng canagliflozin hoặc dapagliflozin. Các yếu tố nguy cơ này bao gồm: khối lượng máu giảm, suy thận mạn tính, suy tim sung huyết hoặc đang dùng các thuốc như: thuốc lợi tiểu, thuốc hạ huyết áp nhóm enzyme (ACE) chuyển đổi angiotensin và thuốc chẹn thụ thể angiotensin (ARB), các thuốc chống viêm không steroid (NSAID); Đánh giá chức năng thận trước khi bắt đầu sử dụng canagliflozin hoặc dapagliflozin và theo dõi định kỳ sau đó. Nếu tổn thương thận cấp tính xảy ra, kịp thời ngừng thuốc và điều trị suy thận.
Canagliflozin và dapagliflozin là thuốc thuộc nhóm cotransporter-2 (SGLT2) ức chế natri-glucose. Đây là thuốc kê đơn được sử dụng cùng với chế độ ăn uống và luyện tập để giúp kiểm soát lượng đường trong máu ở người lớn bị bệnh tiểu đường typ 2. Từ tháng 3/2013, khi canagliflozin đã được phê duyệt, đến tháng 10/2015, FDA đã nhận được báo cáo của 101 trường hợp bị tổn thương thận cấp tính, một số phải nhập viện và lọc máu. Trên thực tế còn nhiều trường hợp xảy ra mà không được báo cáo. Trong khoảng một nửa số trường hợp trên, các biểu hiện của tổn thương thận cấp tính xảy ra trong vòng 1 tháng sau khi bắt đầu dùng thuốc và hầu hết các bệnh nhân được cải thiện sau khi ngừng thuốc. Một số trường hợp xảy ra ở bệnh nhân trẻ hơn 65 tuổi. Nhưng cũng có một số xảy ra ở bệnh nhân bị mất nước, huyết áp thấp hoặc đang dùng các loại thuốc khác có thể ảnh hưởng đến thận.

