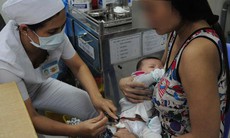
Các trường hợp cần đánh giá nguyên nhân tai biến sau tiêm chủng gồm: trường hợp tai biến nặng sau tiêm chủng; chùm phản ứng vượt quá số lượng thống kê về phản ứng chung của Tổ chức y tế thế giới hoặc có mức độ nghiêm trọng ảnh hưởng đến cộng đồng.
Đó là một trong những nội dung của quyết định " Hướng dẫn giám sát, điều tra, phân tích, đánh giá nguyên nhân phản ứng sau tiêm chủng" của Bộ Y tế do Thứ trưởng Bộ Y tế Nguyễn Thanh Long vừa ký ban hành gửi các cơ sở tiêm chủng trong cả nước
Theo Bộ Y tế phản ứng sau tiêm chủng là hiện tượng bất thường về sức khỏe, bao gồm các biểu hiện tại chỗ về tiêm chủng hoặc toàn thân xảy ra sau khi tiêm chủng, gồm phản ứng thông thường sau tiêm chủng và tai biến nặng sau tiêm chủng. Do đó, giám sát phản ứng sau tiêm chủng bao gồm theo dõi, phát hiện, xứ trí và báo cáo các phản ứng sau tiêm chủng để giảm bớt tác động không tốt đến sức khỏe của người được tiêm chủng.
Các phản ứng sau tiêm chủng gồm có hai loại: Phản ứng thông thường và nhẹ: Phản ứng tại chỗ: sưng, nóng, đỏ, đau; Phản ứng toàn thân: sốt, dễ bị kích thích, cảm giác khó chịu… Tuy nhiên các phản ứng này thông thường là nhẹ và tự khỏi. Đối với phản ứng nghiêm trọng- tai biến nặng sau tiêm chủng bao gồm các triệu chứng như khó thở, sốc phản vệ hay hội chứng sốc phản vệ, hội chứng sốc nhiễm độc, sốt cao, co giật, trẻ khóc kéo dài, tím tái, ngừng thở.
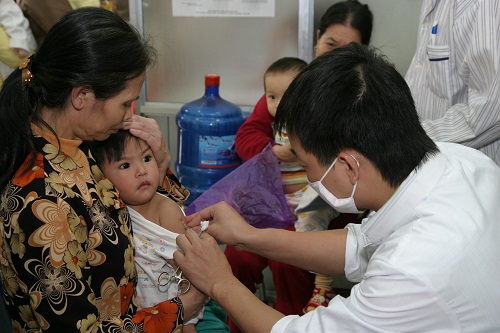
Theo dõi phản ứng sau tiêm chủng để giảm bớt tác động không tốt đến sức khỏe người được tiêm chủng.
Ảnh T.M
Trước đó, liên quan đến công tác tiêm chủng, Bộ Y tế tại cũng đã ban hành thông tư 12 hướng dẫn, khi đang triển khai tiêm chủng mà xảy ra tai biến nặng sau tiêm chủng, người đứng đầu cơ sở tiêm chủng phải chỉ đạo dừng ngay buổi tiêm chủng; xử trí cấp cứu, chẩn đoán nguyên nhân tai biến nặng sau tiêm chủng; trường hợp vượt quá khả năng thì phải chuyển người bị tai biến nặng sau tiêm chủng đến bệnh viện gần nhất. Bên cạnh đó, phải ghi chép đầy đủ thông tin về người được tiêm (bố mẹ - nếu là trẻ em); ngày, giờ tiêm chủng; loại vắc xin tên vắc xin, số lô, hạn dùng, nhà sản xuất, đơn vị cung cấp vắc xin, số đăng ký lưu hành hoặc số giấy phép nhập khẩu. Ghi rõ ngày, giờ xuất hiện tai biến nặng sau tiêm chủng; các triệu chứng chính; kết quả điều trị; kết luận nguyên nhân (nếu có).
Đồng thời cơ sở tiêm chủng phải thống kê toàn bộ số lượng vắc xin đã sử dụng trong buổi tiêm chủng; số người đã được sử dụng theo loại vắc xin; tên vắc xin, số lô, hạn dùng của vắc xin; tình trạng sức khỏe của những người đã được tiêm chủng. Thống kê toàn bộ số vỏ lọ vắc xin, bơm kim tiêm đã sử dụng trong buổi tiêm chủng. Báo cáo tuyến trên theo quy định.
Trong 24 giờ kể từ khi xảy ra trường hợp tai biến nặng sau tiêm chủng, Sở Y tế có trách nhiệm tổ chức điều tra, đánh giá nguyên nhân. Trường hợp nguyên nhân dẫn đến tai biến nặng nghi nhờ do chất lượng vắc xin, Giám đốc Sở Y tế quyết định tạm dừng sử dụng trên địa bàn quản lý lô vắc xin liên quan đến tai biến nặng sau tiêm chủng trên cơ sở ý kiến đồng ý của Cục Quản lý Dược – Bộ Y tế. Khi có kết luận không liên quan đến chất lượng vắc xin, Giám đốc Sở Y tế quyết định việc cho phép sử dụng lại lô vắc xin đó và thông báo tới Cục Quản lý Dược – Bộ Y tế.
Thái Bình