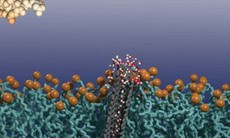
Cảm biến sinh học trong chăm sóc bệnh nhân đái tháo đường
Các hệ thống cảm biến sinh học in vivo tiên tiến nhất đã được sử dụng để theo dõi glucose liên tục (CGM). CGM đã có sẵn trên NHS từ năm 2017 đối với một số người mắc bệnh đái tháo đường týp 1. Thử nghiệm đã cho thấy thiết bị thành công trong việc giảm tỷ lệ hạ đường huyết.
Thiết bị này sử dụng các cảm biến điện hóa được chèn ngay dưới da. Chúng hoạt động trong khoảng 14 ngày, đo nồng độ glucose trong dịch kẽ. Cảm biến sử dụng enzyme glucose oxyase để oxy hóa glucose, tạo thành hydro peroxide phản ứng với platinum bên trong cảm biến.
Sau đó tạo ra tín hiệu điện thay đổi theo nồng độ glucose có thể được gửi không dây đến một thiết bị khác, như điện thoại thông minh hoặc cảm biến khác.
Mục tiêu tiếp theo của hầu hết các công nghệ theo dõi glucose thời gian thực là tạo ra các cảm biến nhỏ hơn và hoạt động lâu hơn, giảm nhu cầu về các quy trình cấy ghép liên tục. Một con đường tiềm năng của nghiên cứu là khám phá các phương pháp quang học; hệ thống first light-based CGM, Eversense ®, đã được Cục quản lý Thuốc và Thực phẩm Hoa Kỳ (FDA) phê duyệt có thể được sử dụng trong 90 ngày. Cảm biến được phủ một hóa chất huỳnh quang tạo ra ánh sáng thay vì tín hiệu điện. Lượng ánh sáng được đo và báo lại cho một ứng dụng trên điện thoại thông minh.

Cảm biến quang học thay đổi màu sắc khi nồng độ của thuốc hoặc ion thay đổi
4 cảm biến sinh học trong tương lai
1. Cảm biến sinh học ionophore dưới da
Kevin Cash, kỹ sư hóa học tại Trường Mỏ Colorado (Mỹ) và các đồng nghiệp đã thiết kế một số cảm biến đo tín hiệu quang hoặc huỳnh quang. Cash đã bắt đầu phát triển các cảm biến quang học tại phòng thí nghiệm tại Đại học Đông Bắc, Boston, Massachusetts. Tín hiệu quang được phát hiện đơn giản bằng cách chụp ảnh bề mặt của da để ghi lại hình ảnh của ánh sáng trong cơ thể được tạo ra.
Về cơ bản, chỉ cần chụp một bức ảnh và có thể biết được những gì đang diễn ra trong cơ thể.

Kevin Cash, gọi cảm biến quang học dựa trên ionophore của mình là "hình xăm hạt nano" vì chúng nằm trong các lớp da.
Một trong những thành công sớm nhất của các nhà khoa học là một cảm biến được theo dõi nồng độ histamine trong cơ thể bằng cách sử dụng enzyme diamine oxidease và một cảm biến nano oxy huỳnh quang. Các histamine bị phá vỡ bởi diamine oxyase, làm giảm nồng độ oxy cục bộ, do đó, làm tăng sự phát quang của chất huỳnh quang nhạy cảm với oxy.
Cash gọi các cảm biến quang học dựa trên ionophore của mình là "hình xăm hạt nano" vì chúng nằm dưới các lớp da. "Chúng có rất nhiều, nhỏ hơn nhiều so với tóc người và chúng ta có thể làm cho mỗi một hạt trong số chúng thay đổi màu sắc khi nồng độ của thuốc hoặc ion hoặc chất chuyển hóa thay đổi", Cash giải thích.
Những cảm biến này có thể phát hiện các ion như lithium, kali, natri và canxi - tất cả được xác định trong sàng lọc chuyển hóa máu tiêu chuẩn. Mặc dù các cảm biến đo nồng độ xen kẽ của các ion này và các phân tử nhỏ khác, thay vì nồng độ của chúng trong máu, nhưng hai giá trị này tỷ lệ thuận với nhau.
2. Cảm biến ống nano carbon phát hiện viêm trong cơ thể
Michael Strano, kỹ sư hóa học tại Viện Công nghệ Massachusetts ở Cambridge, Massachusetts và các thành viên đang độc lập thiết kế các thiết bị ống nano carbon.
Để tạo ra cảm biến, ông Strano đã tạo ra phân tử pha corona, trong đó ống nano được bọc bằng một loại polymer có chức năng.
Các thiết bị đã được chứng minh là hoạt động thành công trên chuột trong tối đa 300 ngày, mang lại hy vọng cho các hệ thống cảm biến dài hạn không cần phải thay thế liên tục.

Gili Bisker, đang độc lập thiết kế các cảm biến ống nano carbon của riêng mình.
Nhà nghiên cứu Gili Bisker, cho hay: Chiều dài bước sóng mà ống nano carbon phát ra dài và không thể nhìn thấy chúng bằng mắt thường. Tuy nhiên, đây là dải quang phổ hoàn hảo cho các công việc trong cơ thể bởi vì ở dải màu này của quang phổ thì cả máu và nước đều không hấp thụ nhiều, vì vậy có thể nhìn sâu hơn vào mô.
Các cảm biến đã được thiết kế để theo dõi oxit nitric, cung cấp dấu hiệu của viêm trong cơ thể và các phân tử khác cũng có thể được phát hiện…
Nhược điểm chính của phương pháp này là mối lo ngại về độc tính của ống nano carbon ở người. Nhưng người ta đã chứng minh rằng khi các bề mặt ống nano bị biến đổi hóa học, độc tính này có thể được ngăn chặn.
3. Cảm biến cung cấp hình ảnh tương tự như siêu âm
Opto-acoustics có thể cung cấp khả năng hình ảnh tương tự như siêu âm.
Jesse Jokerst, một nhà nghiên cứu nano tại Đại học California San Diego, đã tạo ra một ống thông thông minh để theo dõi mức độ heparin chống đông máu trong bệnh nhân. Khoảng 500 triệu liều heparin được tiêu thụ trên toàn cầu mỗi năm. Nhưng việc quản lý gặp rất nhiều khó khăn vì liệu điều trị hẹp, đặc biệt là trẻ em. Liều lượng không chính xác dẫn đến xuất huyết hoặc đông máu. Jokerst đã bọc một ống thông kết hợp với phân tử xanh metylen, được liên kết với heparin và làm tăng đáng kể tín hiệu quang điện của nó.
Ý tưởng là đặt ống thông này vào tĩnh mạch của bệnh nhân. Bệnh nhân sẽ đeo một đầu dò siêu âm linh hoạt ở phía trên cánh tay nơi đặt ống thông tĩnh mạch và sử dụng nó để theo dõi liên tục heparin thay vì chỉ đo mỗi 12 đến 24 giờ.
4. Cảm biến aptamer theo dõi thuốc
Đối với hầu hết các hệ thống, cần có một quá trình phát triển dài cho mỗi cảm biến. Hệ thống có thể được sửa đổi để cảm nhận các loại thuốc hoặc phân tử sinh học khác nhau mà không cần thêm thuốc thử.
Kevin Plaxco, một nhà hóa học từ Đại học California Santa Barbara, tự tin có thể tạo ra một hệ thống như vậy, dựa trên các aptamer - các chuỗi DNA hoặc RNA đơn.
Phân tử chất oxy hóa khử cho phép các electron di chuyển hiệu quả đến điện cực của cảm biến, nhưng sự thay đổi về hình dạng lớn trong phân tử aptamer ảnh hưởng đến khoảng cách giữa chất oxy hoá khử và điện cực, do đó kích thước của tín hiệu này có thể được sử dụng để tính nồng độ chất cần phân tích và không xảy ra các phản ứng hóa học liên quan khác.
Cảm biến aptamer và các điện cực đi kèm tạo ra một thiết bị có kích thước tương đương với tóc người và dễ dàng được cấy trong cơ thể, nhưng cũng đủ nhỏ để được tiêm vào ống thông trong tĩnh mạch. Điều này cho phép khả năng ghi lại các thông số dược động học đầy đủ trong nhiều giờ, với tốc độ lấy mẫu hai giây một lần.
Một lĩnh vực mà nhóm các nhà khoa học đã điều tra là nồng độ kháng sinh trong cơ thể. Trong các thí nghiệm trên động vật, Plaxco đã ghép một cảm biến cho tombramycin vào một hệ thống phân phối thuốc và có thể điều chỉnh nồng độ của thuốc trong huyết tương của động vật.
Cho đến nay các cảm biến chỉ được thử nghiệm trên chuột. Nhưng trong tương lai, rất có khả năng sẽ có khả năng ứng dụng ở người.
Cảm biến sinh học có thể cải thiện các chẩn đoán
Cảm biến trong cơ thể cũng có tiềm năng chẩn đoán và các loại thiết bị này có thể trở thành thiết bị đầu tiên được sử dụng trong các đơn vị cấp cứu hoặc chuyên sâu, chẩn đoán nhanh và cung cấp nhiều thông tin hơn.
Một loại cảm biến sinh học chẩn đoán trong cơ thể khác cũng đang được thiết kế và có thể hạn chế nhu cầu sinh thiết xâm lấn. Gabriel Kwong, tại Học viện Công nghệ Georgia ở Atlanta, Georgia, đã thành lập công ty Glympse Inc, để phát triển chẩn đoán dựa trên cái mà ông gọi là "dấu ấn sinh học tổng hợp".
Hệ thống Kwong đang phát triển sử dụng các hạt nano có chứa các peptide có thể bị phân cắt bởi các protease liên quan đến các bệnh cụ thể. Các hạt nano được tiêm vào bệnh nhân và khi đến môi trường vi mô bị bệnh, các protease liên quan đến bệnh sẽ giải phóng các mảnh peptide nhỏ.
Các nghiên cứu trên chuột đã chỉ ra rằng có thể sử dụng phương pháp này để theo dõi bệnh xơ gan không xâm lấn (phản ứng chữa lành vết thương đối với tổn thương gan mạn tính) và phát hiện ung thư đại trực tràng giai đoạn sớm (phát hiện bệnh trước khi nó xuất hiện dấu ấn sinh học máu).
Kwong nói rằng phương pháp này có thể xác định tiến trình của bất kỳ bệnh nào thay vì chỉ lấy được các thông tin tạm thời riêng lẻ mà sinh thiết cung cấp.
Mời độc giả xem thêm video đang được quan tâm:
Phòng bệnh Bệnh viện Dã chiến đa tầng Tân Bình