Một nghiên cứu mới được công bố trên tạp chí ung thư JAMA của Hiệp hội Y khoa Hoa Kỳ cho thấy: Các bệnh nhân ung thư phổi di căn khi được điều trị phối hợp giữa liệu pháp miễn dịch với các thuốc ức chế điểm kiểm soát (checkpoint inhibitors - CPIs) và xạ trị ngực (thoracic radiotherapy - TRT) đã chứng minh có sự khác biệt về tác dụng miễn dịch so với những người chỉ được điều trị bằng liệu pháp miễn dịch với các thuốc ức chế điểm kiểm soát.
Thuốc ức chế điểm kiểm soát giúp tăng cường hệ miễn dịch
Một phần quan trọng trong cơ chế chống lại bệnh ung thư của hệ thống miễn dịch là khả năng phân biệt giữa các tế bào bình thường trong cơ thể và những tế bào ung thư. Điều này cho phép hệ thống miễn dịch tấn công các tế bào ung thư mà không làm ảnh hưởng đến các tế bào bình thường. Để làm được điều này, các tế bào lympho T trong hệ thống miễn dịch cần có các protein được gọi là “điểm kiểm soát”. PD-1 là một loại protein như vậy. Protein PD-1 nằm trên tế bào lympho T và hoạt động như một loại “công tắc kiểm soát” được gắn kết với PD-L1 (một protein xuyên màng khác có trên các tế bào bình thường). Khi PD-1 liên kết với PD-L1, về cơ bản, tế bào lympho T sẽ nhận định rằng không có mối nguy hại. Chính từ lý do này, một số tế bào ung thư đột biến cũng có số lượng lớn PD-L1 giúp chúng tránh được cuộc tấn công miễn dịch. Các kháng thể đơn dòng nhắm đến đích PD-1 hoặc PD-L1 có thể ngăn chặn sự gắn kết này và tăng cường phản ứng miễn dịch đối với các tế bào ung thư.
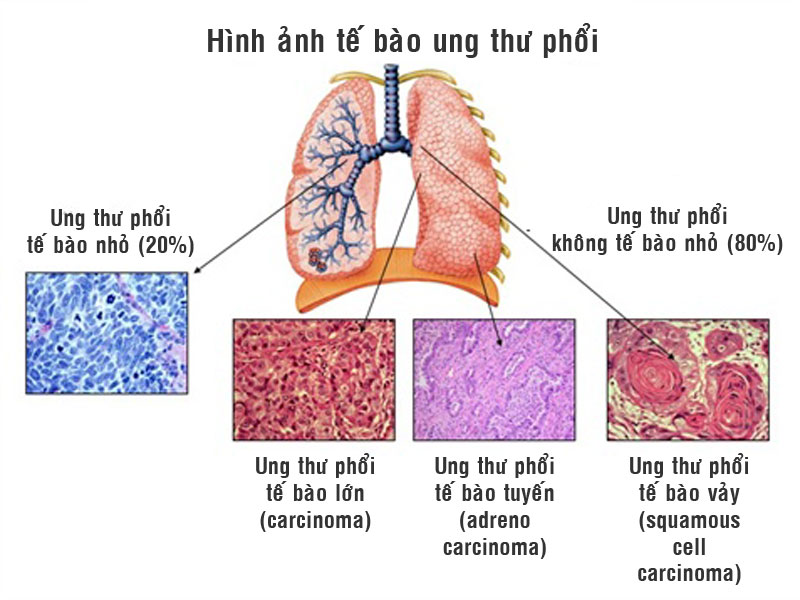 Hình ảnh ung thư phổi.
Hình ảnh ung thư phổi.
Các thuốc ức chế PD-1 bao gồm: pembrolizumab, nivolumab sử dụng trong điều trị ung thư da ác tính, ung thư phổi không tế bào nhỏ (NSCLC), ung thư thận, ung thư bàng quang, ung thư vùng đầu và cổ và u lympho Hodgkin.
Các thuốc ức chế PD-L1 bao gồm: atezolizumab, avelumab, durvalumab sử dụng trong điều trị ung thư bàng quang, ung thư phổi không phải là tế bào nhỏ và ung thư tế bào Merkel.
TS. Florence Keane - Bệnh viện đa khoa Massachusetts, Boston (Hoa Kỳ), tác giả chính của nghiên cứu cho biết: Các thuốc ức chế điểm kiểm soát đã mang lại bước tiến mới trong điều trị bệnh nhân ung thư phổi di căn, cải thiện đáng kể tỉ lệ sống còn chung và tỉ lệ sống còn không tiến triển bệnh so với hóa trị và được cân nhắc cho lựa chọn điều trị đầu tiên trên đa số bệnh nhân ung thư phổi di căn có PD-L1 ≥ 50% hoặc lựa chọn thứ hai sau khi bệnh nhân không đáp ứng với hóa trị liệu.
Tuy nhiên, các thuốc ức chế điểm kiểm soát này cũng có thể tác động tới các cơ quan khác trong cơ thể và gây nên nhiều tác dụng phụ đáng lo ngại. Chẳng hạn như thể nhẹ là: mệt mỏi, buồn nôn, phát ban và ngứa hoặc nặng hơn là các vấn đề trên phổi, gan, thận và nhiều cơ quan khác.
Cả xạ trị ngực và liệu pháp miễn dịch với các thuốc ức chế điểm kiểm soát đều có liên quan đến nguy cơ viêm phổi nên mối quan tâm lớn của các nhà khoa học là: liệu việc sử dụng đồng thời cả hai liệu pháp có làm gia tăng đáng kể nguy cơ các tác dụng phụ miễn dịch bất lợi, đặc biệt là viêm phổi hay không? Đây là rào cản rất lớn trong điều trị ung thư phổi, bởi đa số bệnh nhân được phát hiện muộn và thường không đủ thể lực để vượt qua các tác dụng phụ gặp phải khi sử dụng các liệu pháp xạ trị hay hóa trị, tiên lượng thường xấu và tỉ lệ sống thêm 5 năm thấp.Nhưng qua nghiên cứu này, các nhà khoa học nhận thấy rằng không có sự khác biệt đáng kể về tỉ lệ các tác dụng phụ miễn dịch bất lợi, bao gồm viêm phổi, giữa những bệnh nhân được điều trị xạ trị ngực kết hợp với các thuốc ức chế điểm kiểm soát.
Tác dụng phụ miễn dịch bất lợi mang lại cơ hội tốt cho bệnh nhân
Nghiên cứu được tiến hành trên 164 bệnh nhân ung thư phổi di căn, hầu hết đều bị ung thư phổi không tế bào nhỏ (NSCLC). Tất cả 164 bệnh nhân này đều được điều trị theo liệu pháp miễn dịch với các thuốc ức chế điểm kiểm soát tại bệnh viện đa khoa Massachusetts. Thêm vào đó, 73 bệnh nhân được xạ trị ngực và 91 bệnh nhân không xạ trị. Trong số những bệnh nhân được điều trị phối hợp giữa liệu pháp miễn dịch với các thuốc ức chế điểm kiểm soát và xạ trị ngực (nhóm điều trị kết hợp), giảm 49% tử vong so với 75% ở những người chỉ điều trị bằng liệu pháp miễn dịch với các thuốc ức chế điểm kiểm soát (nhóm điều trị bằng thuốc ức chế điểm kiểm soát). Trong đó, tỉ lệ các tác dụng phụ miễn dịch bất lợi ở mức 2 trở lên rất tương đồng giữa hai nhóm: 13,7% đối với nhóm điều trị kết hợp và 15,4% đối với nhóm điều trị bằng thuốc ức chế điểm kiểm soát. Không có sự khác biệt thống kê trong bất kỳ điểm cuối nào của các tác dụng phụ miễn dịch bất lợi giữa hai nhóm.
TS. Florence Keane giải thích, có một số lý do khiến tỉ lệ sống còn cao hơn ở những bệnh nhân có xuất hiện các tác dụng phụ miễn dịch bất lợi từ mức 2 trở lên trong một loạt phân tích hiện tại so với những bệnh nhân không xuất hiện các tác dụng phụ miễn dịch bất lợi. Một là nguy cơ xuất hiện tác dụng phụ có thể liên quan đến thời gian tiếp xúc với liệu pháp miễn dịch. Các bệnh nhân đang đáp ứng tốt với liệu pháp miễn dịch sẽ tiếp tục liệu trình điều trị, do đó làm tăng nguy cơ độc tính tiềm ẩn. Hai là một số bệnh nhân có xu hướng phát triển phản ứng viêm khi sử dụng các thuốc ức chế điểm kiểm soát dẫn đến sự xuất hiện các tác dụng phụ bất lợi và cải thiện đáp ứng điều trị một cách lâu dài. Ví dụ, trong một phân tích hồi cứu ở những bệnh nhân ung thư hắc tố, các nhà nghiên cứu đã báo cáo một mối liên hệ giữa sự phát triển các phản ứng phụ liên quan đến điều trị và tỉ lệ đáp ứng tổng thể cũng như tỉ lệ sống còn chung, ngay cả khi kiểm soát số lần hóa trị liệu với các thuốc ức chế điểm kiểm soát.
TS. Florence Keane kết luận: “Dữ liệu của nghiên cứu này đã tạo ra giả thuyết mới. Những nghiên cứu ở các giai đoạn di căn và chưa di căn sẽ giúp xác định thời gian tối ưu của xạ trị kết hợp với liệu pháp miễn dịch cũng như theo dõi các độc tính tiềm ẩn”.