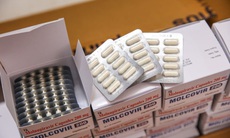
Đến nay, Bộ Y tế đã phân bổ hơn 300.000 liều thuốc Molnupiravir cho 51 địa phương đang triển khai Chương trình sử dụng thuốc có kiểm soát thuốc Molnupiravir cho các trường hợp mắc COVID-19 thể nhẹ tại cộng đồng.
Trước đó, căn cứ kết quả đánh giá giữa kỳ của các nghiên cứu thử nghiệm lâm sàng tiến hành tại Bệnh viện Thống Nhất, Bệnh viện Phổi Trung ương, Đại học Y Dược TP HCM cho thấy tính an toàn và hiệu quả thuốc Molnupiravir, Bộ Y tế đã cho phép triển khai Chương trình sử dụng thuốc có kiểm soát Molnupiravir cho các trường hợp mắc COVID-19 thể nhẹ tại cộng đồng tại TP HCM từ giữa tháng 8/2021 và hiện nay đã mở rộng triển khai tại 51 địa phương có dịch trong toàn quốc.
51 tỉnh, thành sử dụng thuốc Molnupiravir trong điều trị COVID-19 có kiểm soát tại cộng đồng.
Các kết quả báo cáo giữa kỳ của chương trình tại 22 tỉnh/thành phố cho thấy thuốc Molnupiravir có tính an toàn cao, dung nạp tốt, hiệu quả rõ rệt về giảm tải lượng virus, giảm lây lan, giảm chuyển nặng, rút ngắn thời gian điều trị với tỷ lệ bệnh nhân có kết quả xét nghiệm RT-PCR sau 5 ngày âm tính hoặc dương tính với giá trị CT ≥ 30 từ 72,1% đến 99,1%; tỷ lệ bệnh nhân có kết quả xét nghiệm RT-PCR sau 14 ngày âm tính hoặc dương tính với giá trị CT ≥ 30 gần 100%; tỷ lệ chuyển nặng rất thấp từ 0,02%-0,06% và không có ca nào dẫn đến tử vong.
Liên quan đến thuốc Molnupiravir, Bộ Y tế cũng cho biết vừa qua có 10 đơn vị nộp hồ sơ đề nghị cấp số đăng ký cho thuốc chứa hoạt chất Molnupiravir nội.
Trong nghị quyết của Ủy ban Thường vụ Quốc hội vừa ký và có hiệu lực thực hiện ngay từ ngày 30/12, lần đầu tiên có nhiều chính sách đặc biệt được cho phép thực hiện để chống dịch, trong đó có việc sản xuất các thuốc mới điều trị COVID-19.
Nghị quyết giao Bộ trưởng Bộ Y tế xem xét quyết định việc sử dụng dược chất đã được cấp phép nhập khẩu để sản xuất thuốc. Bộ trưởng Bộ Y tế xem xét, quyết định việc sử dụng dược chất đã được cấp phép nhập khẩu theo quy định của pháp luật về dược cho mục đích khác để sản xuất thuốc đã được cấp giấy đăng ký lưu hành và có chỉ định sử dụng phòng, điều trị COVID-19;
Trường hợp thiếu thuốc phòng, điều trị COVID-19, Bộ trưởng Bộ Y tế quyết định việc sử dụng miễn phí thuốc sản xuất trong nước thuộc lô được sản xuất để phục vụ cấp giấy đăng ký lưu hành thuốc có chỉ định sử dụng phòng, điều trị COVID-19 nếu đáp ứng đồng thời các điều kiện: Được sản xuất theo đúng quy trình sản xuất trong hồ sơ đăng ký lưu hành thuốc đã được Bộ Y tế thẩm định và cấp giấy đăng ký lưu hành; Đáp ứng tất cả các nội dung như hồ sơ đăng ký lưu hành thuốc đã được Bộ Y tế phê duyệt; Được sự đồng ý của cơ sở sản xuất thuốc.
Các thuốc mới có chỉ định điều trị COVID-19 nhập khẩu, được cấp phép có điều kiện tại một trong số cơ quan quản lý thuốc SRA (Tổ chức Y tế thế giới công bố) được cấp phép trong 10 ngày.
Các thuốc mới có chỉ định điều trị COVID-19 sản xuất trong nước nếu có cùng dạng bào chế, đường dùng, hàm lượng với thuốc đã được SRA cấp phép thì Việt Nam cho phép miễn nộp hồ sơ nghiên cứu lâm sàng.
Đối với giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc hết hiệu lực trong khoảng thời gian từ ngày Nghị quyết này có hiệu lực đến trước ngày 31 tháng 12 năm 2022 mà không thể thực hiện kịp thời thủ tục gia hạn đăng ký lưu hành do ảnh hưởng của dịch COVID-19 thì được tiếp tục sử dụng đến hết ngày 31 tháng 12 năm 2022 để bảo đảm phục vụ công tác khám bệnh, chữa bệnh.
Đến nay Việt Nam đã đưa vào sử dụng nhiều loại thuốc trong điều trị bệnh nhân COVID-19 như thuốc ức chế sự nhân lên của virus: Molnupiravir, Remdesivir, Favipiravir,... Ngoài ra thuốc kháng thể kép cũng đang được đưa vào điều trị cho bệnh nhân COVID-19 nặng.
Các thuốc hỗ trợ khác như thuốc ức chế phản ứng miễn dịch (Chất ức chế Interleukin-6, Baricitinib), thuốc chống đông, kháng sinh, kháng nấm, thuốc dược liệu, thuốc cổ truyền cũng được đưa vào phục vụ điều trị bệnh nhân COVID-19…