Việt Nam sản xuất thành công vắcxin sởi - rubella
Vắcxin sởi - rubella (MRVAC) do POLYVAC sản xuất được chính phủ Nhật Bản hỗ trợ chuyển giao kỹ thuật theo yêu cầu của chính phủ Việt Nam. Sản phẩm được cty Kitasato Daiichi Sankyo Vắc xin - Nhật Bản chuyển giao công nghệ.
MRVAC là vắcxin phối hợp bao gồm 2 thành phần: virút sởi sống, giảm độc lực và kháng nguyên Rubella. Vắcxin MRVAC có thành phần kháng nguyên virút sởi và tá dược giống như vắcxin MVVAC (cũng do POLYVAC sản xuất và do cty Kitasato chuyển giao công nghệ; được lưu hành và cung ứng trong chương trình tiêm chủng mở rộng từ năm 2010 tới nay với khoảng 30 triệu liều vắcxin đã được sử dụng). Vắcxin MRVAC chỉ bổ sung kháng nguyên Ruballa vào vắcxin MVVAC.
Dây chuyền sản xuất vắcxin MRVAC của POLYVAC đã đạt chứng nhận thực hành tốt sản xuất WHO-cGMP do Bộ Y tế cấp. Vắcxin MRVAC được Bộ Y tế cấp số đăng ký lưu hành số QLVX-995-17 này 27/3/2017.

Việc sử dụng vắcxin sởi - rubella MRVAC sản xuất trong nước sẽ giúp Việt Nam chủ động nguồn cung ứng vắcxin, đảm bảo không thiếu vắcxin Sởi - Rubella sử dụng trong tiêm chủng thường xuyên cho trẻ 18 tháng tuổi và tiêm chủng chống dịch trên quy mô toàn quốc. Trong tháng 2/2018, MRVAC đã được đưa vào sử dụng trong chương trình tiêm chủng mở rộng, bước đầu triển khai tại 4 tỉnh Nam Định, Khánh Hòa, Đắk Nông và Bà Rịa - Vũng Tàu, trong buổi tiêm chủng thường xuyên cho trẻ 18 - 24 tháng. Theo báo cáo của 4 tỉnh, đã có 7.787 trẻ từ 18 - 24 tháng tuổi được tiêm MRVAC, không ghi nhận trường hợp phản ứng nặng sau tiêm. Kết quả thu được cho thấy tính an toàn của MRVAC tương tự với vắcxin sởi - rubella do Ấn Độ sản xuất đã sử dụng như giai đoạn 2014 - 2016.
Từ tháng 4/2018, vắcxin MRVAC do Việt Nam sản xuất được triển khai trong tiêm chủng thường xuyên trên toàn quốc. Đến nay, 19 tỉnh/thành triển khai bao gồm: Nam Định, Hà Nội, Bắc Ninh, Bắc Giang, Lạng Sơn, Thanh Hóa, Khánh Hòa, Quảng Nam, Đà Nẵng, Quảng Trị, Phú Yên, Ninh Thuận, Đắk Nông, Bà Rịa - Vũng Tàu, Đồng Tháp, Tây Ninh, Trà Vinh, Bình Dương, Bình Phước Theo báo cáo của các tỉnh, đã có trên 50.000 trẻ từ 18 - 24 tháng tuổi được tiêm vắcxin MRVAC, không ghi nhận bất kỳ trường hợp phản ứng nặng sau tiêm chủng nào.
Vắcxin bại liệt tiêm
Việt Nam, trước khi có vắcxin phòng bệnh, bệnh bại liệt là một trong những nguyên nhân gây tử vong hàng đầu và để lại di chứng nặng nề ở trẻ dưới 5 tuổi. Nhờ triển khai uống vắcxin phòng bệnh bại liệt và nhiều năm duy trì ở tỉ lệ uống vắcxin cao trên 90%, bệnh bại liệt đã dành dược khống chế, ca bệnh cuối cùng được ghi nhận tại Việt Nam năm 1997. Việt Nam đã chính thức công bộ thanh toán bệnh bại liệt vào năm 2000 và từ đó đến nay vẫn đang duy trì thành quả này.
Tuy nhiên, bệnh bại liệt vẫn chưa được thanh toán trên quy mô toàn cầu. Hiện virút bại liệt hoang dại vẫn còn lưu hành ở một số nước (Afghanistan, Pakistan…). Thực hiện chiến lược của Tổ chức Y tế Thế giới (WHO), Bộ Y tế đã phê duyệt kế hoạch “Bảo vệ thành quả thanh toán bại liệt ở Việt Nam giai đoạn 2016 - 2020”, bao gồm triển khai vắcxin bại liệt uống 2 týp (bOPV) và vắcxin bại liệt tiêm (IPV) trong chương trình tiêm chủng mở rộng.
Thực hiện kế hoạch triển khai vắcxin bại liệt uống bOPV (gồm virút týp 1 và týp 3), Việt Nam đã dừng sử dụng vắcxin bại liệt uống 3 týp trên toàn quốc và chuyển đổi sử dụng vắcxin bại liệt uống bOPV từ tháng 6 năm 2016 cho trẻ em dưới 1 tuổi vào lúc 2,3,4 tháng tuổi trong tiêm chủng thường xuyên, đạt 95% trên quy mô toàn quốc.
Năm 2018, vắcxin bại liệt tiêm IPV sẽ được triển khai trong chương trình tiêm chủng mở rộng
WHO khuyến cáo các quốc gia đang sử dụng vắcxin bại liệt uống bOPV thì cần sử dụng thêm 1 liều vắc xin bại liệt tiêm cho trẻ dưới 1 tuổi trong lịch tiêm chủng thường xuyên. Vắcxin bại liệt tiêm là vắcxin bất hoạt, chứa các týp virút bại liệt đã chết, được sử dụng dưới dạng vắcxin tiêm.
Tiêm 1 mũi vắcxin IPV có chứa cả 3 týp kháng nguyên bại liệt týp 1, 2 và 3 giúp tăng cường miễn dịch đối với týp 1 và týp 3 đồng thời gây miễn dịch phòng bệnh đối với týp 2 cho trẻ sử dụng 3 liều bOPV.
Vắcxin IPV sử dụng trong chương trình tiêm chủng mở rộng là vắcxin được sản xuất tại Pháp, được cấp giấy phép đăng ký lưu hành tại Việt Nam. Vắcxin do tổ chức Liên minh Toàn cầu Vắcxin và Tiêm chủng (GAVI) hỗ trợ và được cung ứng bởi quỹ Nhi đồng Liên hiệp quốc (UNICEF).
Để tiếp tục duy trì thành quả thanh toán bại liệt đạt được, thực hiện khuyến cáo của WHO, cùng với tiếp tục cho trẻ 2, 3, 4 tháng tuổi uống 3 liều vắcxin bại liệt bOPV (vắcxin bại liệt 2 týp), từ tháng 8/2018 trẻ sẽ được tiêm 1 mũi vắcxin IPV lúc 5 tháng tuổi trong tiêm chủng thường xuyên.
Chuyển đổi vắc xin phối hợp 5 trong 1
Vắc xin phối hợp các bệnh bạch cầu, ho gà, uốn ván, viêm gan B và viêm phổi/viêm màng não mủ do vi khuẩn Hib (DPT-VGB-Hib) được đưa vào chương trình Tiêm chủng mở rộng từ tháng 6/2010. Hàng năm có khoảng 1,6 - 1,7 triệu trẻ em dưới 1 tuổi được tiêm đủ 3 mũi vắcxin với tỉ lệ đạt trên 95% trên quy mô toàn quốc.
Vắcxin DPT-VGB-Hib sử dụng trong chương trình tiêm chủng mở rộng từ khi bắt đầu triển khai đến nay có tên thương mại Quinvaxem, do cty Berna Biotech, Hàn Quốc sản xuất. Dự án tiêm chủng mở rộng đã sử dụng khoảng 41 triệu liều vắcxin Quinvaxem tiêm chủng miễn phí cho trẻ dưới 1 tuổi. Vắcxin Quinvaxem được sử dụng an toàn và hiệu quả trong tiêm chủng mở rộng, giúp giảm tỉ lệ mắc các bệnh truyền nhiễm nguy hiểm ở trẻ em.
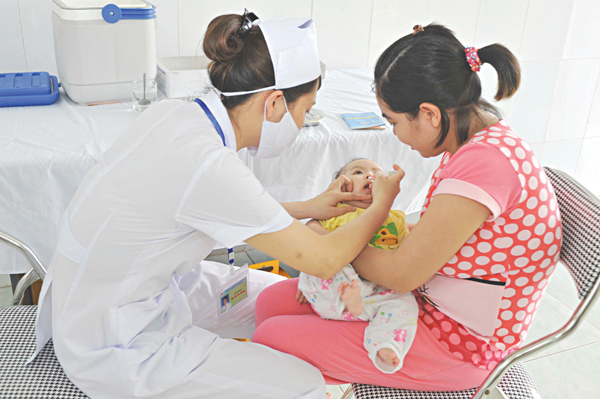 Vắcxin bại liệt uống đã giúp hàng triệu trẻ em phòng chống được căn bệnh này
Vắcxin bại liệt uống đã giúp hàng triệu trẻ em phòng chống được căn bệnh này
Hiện nay, nhà sản xuất Berna Biotech đã ngừng sản xuất vắcxin Quinvaxem, số vắcxin này còn lại trong chương trình tiêm chủng mở rộng dự kiến sẽ sử dụng đến hết tháng 5/2018. Bộ Y tế đã có kế hoạch chuyển đổi sử dụng vắcxin Quinvaxem bằng loại vắcxin phối hợp 5 trong 1 tương tự về thành phần và hiệu quả phòng bệnh. Vắcxin phối hợp 5 trong 1 được lựa chọn để thay thế vắcxin Quinvaxem có tên thương mại là vắcxin ComBe Five do Ấn Độ sản xuất đã được Bộ Y tế cấp phép lưu hành ở Việt Nam từ tháng 5/2017. Vắcxin này có thành phần tương tự như vắcxin Quinvaxem có hiệu quả phòng các bệnh bạch hầu, ho gà, uốn ván, viêm gan B, viêm phổi/viêm màng não mủ do vi khuẩn Hib đạt tiêu chuẩn tiền thẩm định WHO và đã được sử dụng ở hơn 43 quốc gia với hơn 400 triệu liều.
Vắcxin ComBe Five có dạng trình bày tương tự như vắcxin Quinvaxem: vắcxin được đóng 1 liều/lọ và lọ vắcxin có gắn chỉ thị nhiệt độ (VVM) để giám sát việc tiếp xúc với nhiệt độ của từng lọ vắcxin trong quá trình bảo quản, vận chuyển trước khi sử dụng.
Tính an toàn và hiệu quả của vắcxin ComBe Five tương tự như các vắcxin 5 trong 1 có cùng thành phần. Kết quả sử dụng vắcxin ComBe Five tại thực địa 4 huyện của tỉnh Hà Nam năm 2016 ghi nhận một số phản ứng thông thường xuất hiện vào ngày thứ nhất sau tiêm vắcxin, bao gồm phản ứng tại chỗ tiêm đau, quầng đỏ với tỉ lệ 5 - 15%, sốt tỉ lệ 34 - 39%, không ghi nhận bất kỳ phản ứng nghiêm trọng nào sau tiêm chủng.
Dự kiến việc chuyển đổi sử dụng vắc xin DPT-VGB-Hib sẽ được triển khai trên toàn quốc trong tháng 6,7 năm 2018. Trước khi triển khai trên toàn quốc, dự án tiêm chủng mở rộng sẽ triển khai trước tại 4 tỉnh Hà Nam, Bình Định, Kon Tum, Đồng Tháp để có thêm kinh nghiệm về triển khai trên diện rộng tại hơn 11.000 điểm tiêm chủng.
Hiện nay, vắcxin Quinvaxem vẫn tiếp tục được sử dụng cho trẻ dưới 1 tuổi trong chương trình tiêm chủng mở rộng cho tới khi được thay thế bằng vắcxin mới để đảm bảo trẻ em được tiêm chủng đầy đủ. Lịch tiêm chủng vắcxin DPT-VGB-Hib không thay đổi, trẻ dưới 1 tuổi cần được tiêm đủ 3 mũi vào lúc 2, 3 và 4 tháng tuổi. Trẻ em được tiêm 1 hoặc 2 mũi vắcxin Quinvaxem sẽ tiếp tục sử dụng vắcxin ComBe Five cho các mũi tiêm tiếp theo.
Bộ Y tế khuyến cáo các bậc cha mẹ tiếp tục đưa con đi tiêm chủng đầy đủ, đúng lịch các vắcxin trong chương trình tiêm chủng mở rộng, để phòng các bệnh truyền nhiễm nguy hiểm.




